
2023年5月12日,香港伊利沙伯医院心内科Dr. Michael Lee及其团队成功应用JenaValve公司Trilogy经导管主动脉瓣系统为两名外科手术禁忌的重度主动脉瓣反流患者成功完成经股主动脉瓣置换介入治疗。这是该产品在亚洲的首次临床应用,其正式落地并开启香港地区商业化市场,为该地区主动脉瓣关闭不全患者带来全新的安全有效的微创介入治疗选择。

此次接受Trilogy植入的两名患者临床诊断均为症状性重度主动脉瓣反流,且有外科手术禁忌。Dr. Michael Lee与其团队Dr. Ivan Wong, Dr. Angus Chui于术前多次就患者的病情和解剖条件进行详细的分析讨论,,术中使用局部麻醉,顺利完成两台手术,平均器械手术时长仅为25分钟( from sheath-in to sheath-out )。瓣膜植入即刻位置理想,仅轻度及以下瓣周漏,术后血流动力学显著改善。本次手术得到了英国St. Bartholomew’s医院Baumbach教授指导。
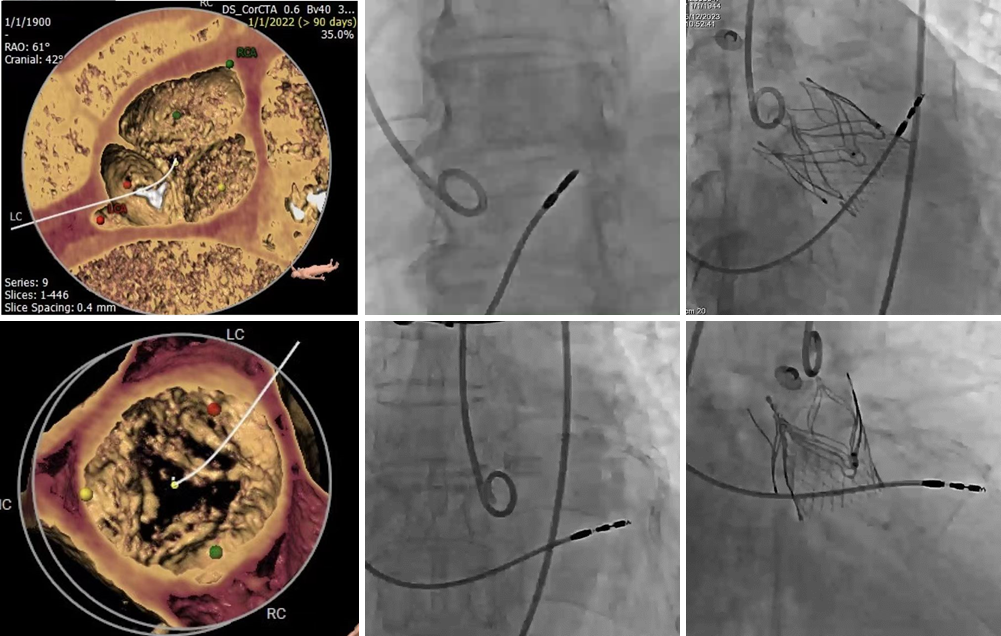
【攻克治疗难题,外科高危禁忌重度主动脉瓣反流迎来经股TAVI解决方案】
《2020 ACC/AHA瓣膜性心脏病患者管理指南》指出,由于主动脉瓣环和主动脉根部扩张,以及患者原生瓣叶钙化不足,采用传统TAVI器械存在瓣膜位移以及瓣周漏的风险,目前经导管主动脉瓣置换术(TAVI) 治疗孤立性慢性主动脉瓣反流具有挑战性。
针对主动脉瓣狭窄设计TAVI器械的off-label应用,在临床实践中存在患者解剖的高选择性,以及对术者团队手术经验的要求严苛性,使得绝大多数这类患者未得到及时、有效治疗。如何针对主动脉瓣反流(AR)患者的解剖特点设计一款手术成功率更高、并发症更低,学习曲线更短的经股TAVI器械,成为亟待满足的临床需求。
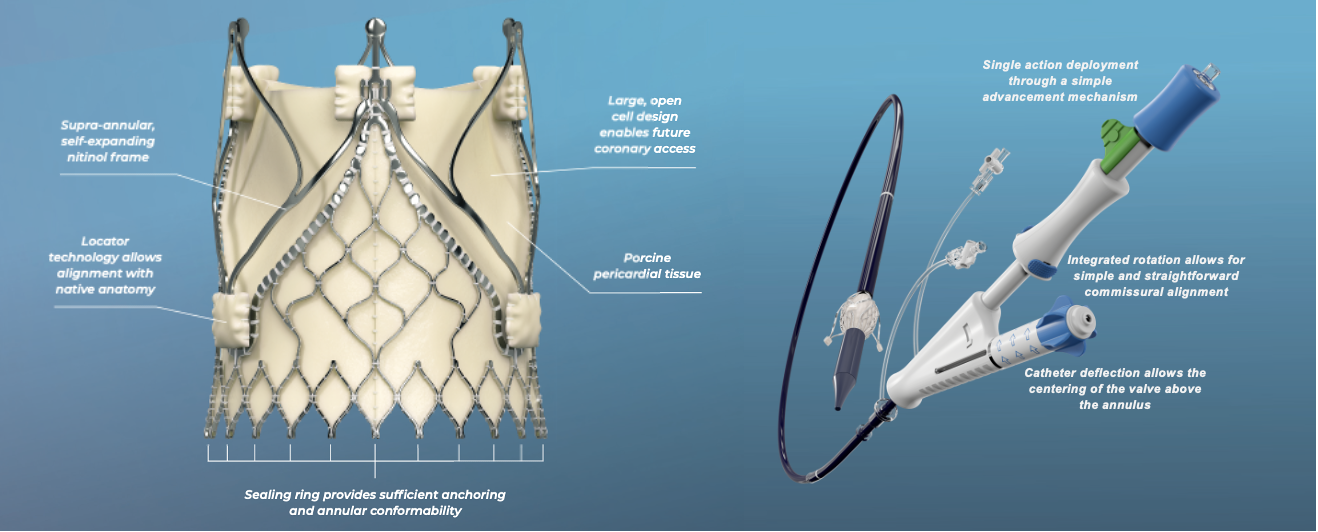
【经股主动脉瓣置换术治疗重度主动脉瓣反流,Trilogy一枝独秀】
JenaValve公司经过十余年探索和技术积累,引领TAVI治疗AR的突破创新,使得Trilogy经导管主动脉瓣系统于2021年获得CE Mark认证,是全球首个获批具有重度主动脉瓣反流与重度主动脉瓣狭窄双适应证的经股动脉入路的瓣膜系统[1]。
Trilogy独有的定位键设计可夹持原生瓣叶,降低瓣膜位移及瓣中瓣等并发症的手术风险。其独特的支架切割工艺实现流入端致密骨架设计,提供锚定与有效封堵;流出端超大网孔,配合输送系统实现对合缘对齐,进一步保障假体瓣膜植入无位移、密封效果及冠脉再介入。
最新公布的欧洲上市后临床数据显示[2],Trilogy AR组手术即刻成功率100%,30天随访结果表明所有患者均为轻度及以下瓣周漏。目前Trilogy已在欧洲多个国家完成百余例商业化植入,在美国ALIGN-AR的FDA临床研究已完成入组,有望成为首个FDA批准的治疗重度主动脉瓣反流的TAVR器械。

【沛嘉医疗致力于将Trilogy前沿技术落地大中华区,多种路径推动技术普及救治患者】
2022年初,沛嘉医疗(9996.HK)和JenaValve公司达成战略合作,在中国大陆,通过license-in实现Trilogy技术一致性自产化,借助沛嘉医疗供应链和产能优势,加速相应产品临床及注册。此外,通过沛嘉医疗的代理渠道,JenaValve快速将Trilogy这一全球独特创新器械落地香港。JenaValve与沛嘉医疗协同资源,期待服务更多大中华区临床中心和患者,满足广大的治疗需求。
【专家寄语,见证经股主动脉瓣置换术治疗重度主动脉瓣反流又一里程碑】

Dr. Michael Lee, Head of Cardiology, Consultant Cardiologist, Queen Elizabeth Hospital, Hong Kong SAR, China
The Trilogy Heart Valve System is a highly innovative therapeutical option licensed for both severe AR and severe AS patients. We are inspired that the Trilogy procedure is quite predictable due to its solid anchoring and the locator technology limiting the displacement, and the results of the first two cases of inoperable AR were successful and satisfying. These two AR cases are the first implantation with on-label TAVI transfemoral system in Asia. We do hope that Trilogy technique could save more patients who are suffering severe AR related disease in the future.

张一博士,沛嘉医疗董事长兼CEO
此次与JenaValve合作,是继签署大中华区独家技术转让后,沛嘉医疗拓展商业化市场版图的重要里程碑。沛嘉医疗致力于通过前沿独特创新技术,服务更多临床中心,让更多创新治疗方案惠及结构性心脏病患者。沛嘉医疗将继续秉承至善尽心敬畏生命的宗旨,以国际化视野致力于打造本土医疗创新生态,推动瓣膜介入领域的创新器械和革命性疗法进一步落地。

John Kilcoyne, JenaValve CEO
We are clearly thrilled about the first commercial implants of the Trilogy Heart Valve System in Hong Kong SAR, China. This marked a major milestone accomplishment for the clinical use of Trilogy in Asia. We look forward to partnering with Peijia Medical and opinion leaders of Greater China to treat more severe, symptomatic aortic regurgitation patients in future.

Peter Spadaro, JenaValve CCO
The Trilogy Heart Valve offers a new option and more importantly an effective option for severe AR patients who historically had very few options for treatment. We are greatly encouraged by the first implants in Hong Kong and will be devoted to the future promotion of Trilogy in Asia. We are happy to see that the cooperation between Jenavalva and Peijia could provide operators with cutting-edge technology, which is aimed at improving the lives of our patients at the top speed.
【参考文献】
[1] JenaValve Technology Receives CE Mark for its Trilogy™ TAVI System for the Treatment of Aortic Regurgitation and Aortic Stenosis. IRVINE, Calif., May 25th, 2021. https://jenavalve.com/jenavalve-receives-ce-mark/.
[2] The Dedicated Jenavalve Trilogy TAVI System for Aortic Regurgitation: Early EU Experiences. Alexander R. Tamm. University Medical Center Mainz, Germany. TCT 2022.
Indication Statement: “The Jenavalve Trilogy Heart Valve System (transfemoral) is indicated for use in patients with symptomatic severe aortic regurgitation (AR) or symptomatic severe aortic stenosis (AS) who are judged by a Heart Team (including a cardiac surgeon), to be at high or greater risk for surgical aortic valve replacement.
CAUTION-Investigational Device. Limited by Federal (or United States) law to investigational use